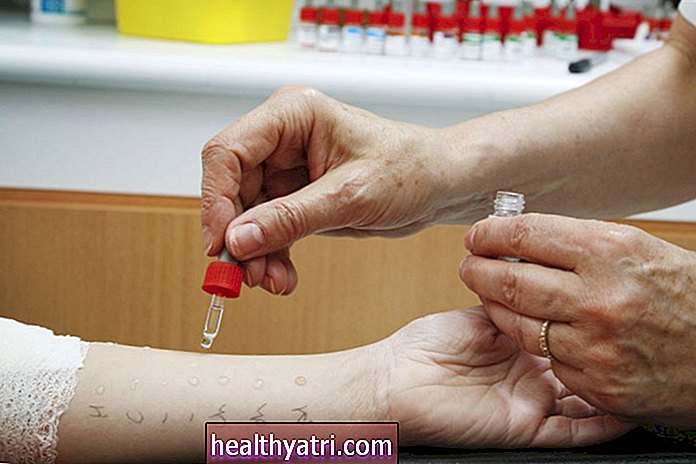
Terapia agnostică tumorală se referă la tratamentele împotriva cancerului care funcționează în toate tipurile de cancer. Cu alte cuvinte, în loc să lucreze pentru un singur tip de cancer, cum ar fi cancerul de sân, aceste tratamente pot funcționa pentru mai multe tipuri de cancer diferite, de exemplu, melanom, cancer de sân și sarcoame. În plus, pot funcționa atât pentru adulți, cât și pentru copii.
Panuwat Dangsungnoon / iStock
În loc de tratamente bazate pe originea unei tumori, această terapie tratează un cancer care își are originea oriunde, pe baza caracteristicilor moleculare particulare care determină creșterea tumorii. În ciuda apariției în diferite țesuturi, nu este neobișnuit ca tipuri foarte diferite de cancer să folosească aceeași cale pentru a crește
O înțelegere sporită a biologiei cancerului, capacitatea de a face teste genomice pentru a determina ceea ce determină creșterea unui anumit cancer și disponibilitatea medicamentelor care vizează aceste căi le-a oferit cercetătorilor capacitatea de a trata o gamă largă de cancere la nivel molecular .
În prezent, există doar câteva medicamente aprobate special pentru tratamentul agnostic al tumorii, dar se așteaptă ca aceasta să se extindă rapid în viitorul foarte apropiat. Vom arunca o privire asupra definiției și importanței tratamentelor agnostice tumorale, exemple care sunt utilizate în prezent și beneficiile și limitările acestei abordări de tratament.
Definirea terapiei agnostice tumorale
Terapia agnostică tumorală se referă la utilizarea medicamentelor pentru a trata un cancer pe baza structurii moleculare a unei tumori, mai degrabă decât la locul de origine al cancerului.
Importanţă
Tratamentele împotriva cancerului au avansat astfel încât, cu tipuri specifice de cancer (de exemplu, cancerul pulmonar), tratamentele sunt deja deseori alese pe baza caracteristicilor moleculare ale tumorii.
De exemplu, în cazul cancerului pulmonar cu celule mici, mai degrabă decât în alegerea tratamentelor în principal pe baza a ceea ce se vede la microscop, testarea genomică (cum ar fi secvențierea generației următoare) permite medicilor să stabilească dacă cancerul are o mutație genică specifică (sau altă modificare ) pentru care terapiile vizate sunt acum disponibile.
În timp ce un anumit medicament pentru chimioterapie poate fi administrat pentru mai multe tipuri de cancer, principiul din spatele tratamentului este diferit. Chimioterapia tratează în esență celulele care se divid rapid.
În schimb, terapiile vizate (și într-un mod diferit, medicamentele de imunoterapie) vizează o cale foarte specifică în creștere. Două tipuri de cancer care sunt de același tip și stadiu și care ar răspunde în mod similar la chimioterapie, pot răspunde foarte diferit la tratamentul cu un medicament vizat.
În cazul în care tumoarea are o mutație, cum ar fi o mutație EGFR, utilizarea unui medicament care vizează mutația (cum ar fi un inhibitor EGFR) este foarte probabil să ducă la controlul creșterii cancerului. În schimb, dacă tumora care nu are această mutație, este puțin probabil să răspundă deloc la inhibitorul EGFR.
Tratamentele care vizează aceste modificări genomice specifice (care este uneori denumită „semnătura moleculară” a tumorii) au schimbat foarte mult atât tratamentul multor tipuri de cancer, cât și accentul pus pe dezvoltarea medicamentelor.
Biologie și terminologie
Pentru a discuta despre tratamentele agnostice tumorale, este util să vorbim despre o parte din biologia confuză. Din fericire, oamenii devin din ce în ce mai împuterniciți și învață despre cancerele lor, dar nu este diferit de învățarea unei limbi străine provocatoare.
Pentru ca un cancer să crească în continuare, celulele trebuie să fie suficient de diferite de celulele normale încât să nu asculte semnalele normale ale corpului pentru a nu mai crește sau a se elimina. Există căi complexe implicate în creșterea celulelor, iar anomaliile din mai multe dintre aceste puncte pot duce la creșterea necontrolată.
Mutațiile genice (și alte modificări) stau la baza cancerului și o serie a acestor mutații duce la transformarea unei celule într-o celulă canceroasă. Genele sunt planul proteinelor, iar proteinele, la rândul lor, sunt agenții care fie stimulează, fie inhibă diferite puncte de pe aceste căi.
Acum există o serie de medicamente (și multe altele în curs de dezvoltare și studii clinice) care inhibă unele dintre aceste proteine și, prin urmare, opresc semnalizarea care duce la creșterea continuă a unui cancer. Câțiva termeni sună foarte confuz, dar sunt destul de simpli atunci când sunt definiți.
Termenul mutație conducător auto se referă la o mutație într-o genă care codifică o proteină care controlează creșterea unui cancer. Cancerele care prezintă această mutație (sau altă modificare) sunt „dependente” de proteina anormală produsă pentru a continua să crească. Oncologii folosesc adesea termenul de dependență de oncogen pentru a descrie acest comportament.
Mutația specială ar fi numită apoi semnătura moleculară a cancerului.
Criterii pentru tratamentele tumorale agnostice
Pentru ca un tratament să fie eficient în toate tipurile de cancer, există puține criterii care trebuie îndeplinite.
- Mutația particulară (sau altă modificare) trebuie găsită. Cu alte cuvinte, testarea trebuie să fie disponibilă pentru a detecta modificarea și să fie efectuată destul de des.
- Tumorile care prezintă mutația specială trebuie să răspundă la tratamentele care vizează tratamentul.
- Mutația trebuie găsită în multe tipuri diferite de cancer.
Utilizări și exemple
În prezent, există câteva medicamente care au fost aprobate pentru utilizarea tumorilor agnostice și altele care sunt utilizate în afara acestui mod. Ne vom uita la unele dintre aceste medicamente.
Keytruda
Keytruda (pembrolizumab) a fost primul medicament aprobat pentru tratamentul agnostic al tumorii în 2017. Ketruda este un anticorp monoclonal PD-clasificat ca punct de control inhitibor (un tip de medicament pentru imunoterapie). răspunsul propriului sistem imunitar al organismului la un cancer.
Keytruda este aprobat pentru tumorile solide la adulți sau copii care prezintă o instabilitate ridicată a microsateliților (MSI-H) sau sunt deficiente în repararea nepotrivirii (dMMR). Fie MSI-H, fie dMMR pot fi găsite cu teste care se fac pe tumoare (PCR sau imunohistochimie).
În 2020, Keytruda a primit o a doua aprobare agnostică tumorală pentru persoanele cu tumori solide care au o sarcină mutațională ridicată. Sarcina mutațională este o măsură a numărului de mutații prezente într-o tumoare canceroasă și este asociată (dar nu întotdeauna) cu un răspuns pozitiv la medicamentele imunoterapice.
Vitrakvi
Vitrakvi (larotrectinib) este al doilea medicament care a primit aprobare pentru tratamentul agnostic al tumorii în 2018. Este aprobat pentru adulți sau copii cu tumori cu proteine de fuziune NTRK. Fuziunea genică a receptorului kinazei neurotrofice (NTRK) se găsește în numai 1% a multor tumori solide, cum ar fi cancerul pulmonar, dar pot fi prezente în până la 60% din unele tipuri de sarcoame.
Unele dintre tipurile de cancer pentru care a fost demonstrat un răspuns includ cancerul pulmonar, melanomul, tumorile GIST, cancerul de colon, sarcoamele țesuturilor moi, tumorile glandei salivare, fibrosarcomul infantil, cancerul de sân și cancerul pancreatic.
La adulții cu tumori care adăpostesc fuziunea genei NTRK, rata de răspuns la Vitrakvi a fost de 75% până la 80%. Într-un studiu separat la copii, rata generală de răspuns a fost de 90%.
Aceste răspunsuri au fost observate chiar și atunci când oamenii au primit tratamente anterioare. Ceea ce face acest lucru este să confirme cât de dependente de această cale sunt aceste tumori pentru creștere. Nu numai că răspunsurile au fost ridicate, dar folosind Vitrakvi a reușit, a câștigat unele cazuri, a permis chirurgilor să efectueze mai puține operații desfigurante la copii.
Rozlytrek
În 2019, FDA a aprobat utilizarea Rozlytrek (entrectinib) pentru persoanele cu tumori care adăpostesc fuziunea genei NTRK, precum și pentru cancerul pulmonar cu celule non-mici, cu o modificare a ROS1.
Medicamentul a fost aprobat pentru adulți sau copii care suferă de cancer metastatic sau pentru care intervenția chirurgicală ar putea duce la o desfigurare semnificativă. În timpul evaluării, răspunsul general rar a fost de 78%.
Cele mai frecvente tipuri de cancer din studiu au fost sarcomul, cancerul pulmonar cu celule mici, cancerul de sân, cancerul colorectal, cancerul tiroidian și cancerul secretor analog mamar.
Mutații BRAF
În timp ce o terapie specifică cu agnostic tumoral nu a fost aprobată, cercetătorii au descoperit că persoanele cu diferite tipuri de cancer care adăpostesc mutații BRAF răspund adesea la tratamentul cu inhibitori BRAF (de obicei în combinație cu un inhibitor MEK).
Mutațiile BRAF au fost inițial observate (și tratate) la persoanele cu melanom metastatic, dar au fost acum demonstrate în cancerul pulmonar cu celule mici (aproximativ 3%), cancerul de colon, leucemia cu celule păroase, cancerul tiroidian, cancerul ovarian seros și altele.
Alte exemple
Deoarece testarea de generația următoare se efectuează mai des, cercetătorii încep să vadă modificări genetice despre care se credea că erau izolate de un tip de cancer în alte tipuri.
De exemplu, modificarea observată cu cancerul de sân HER2 pozitiv este prezentă la unii oameni cu cancer pulmonar.Alte exemple includ utilizarea medicamentului Lynparza (olaparib) nu numai pentru cancerul de sân, ci și pentru cancerul ovarian, cancerul de prostată și cancerul pancreatic care conține o mutație BRCA.
Testare și încercări
Există o serie de medicamente în curs de dezvoltare, precum și cele din studiile clinice în acest moment. Tipurile de studii clinice care uneori evaluează medicamentele din diferite clase de cancer includ studii cu coș și studii umbrelă. Evaluarea este facilitată de un protocol de potrivire de precizie numit NCI-MATCH.
Beneficii și limitări
Există beneficii clare atunci când vine vorba de posibilitatea de a utiliza un singur tratament pentru mai multe tipuri diferite de cancer, dar există și limitări.
Beneficii
Este de la sine înțeles că medicamentele agnostice tumorale au beneficii atunci când vine vorba de cercetarea și dezvoltarea medicamentelor. Dezvoltarea medicamentelor este foarte costisitoare. Cu toate acestea, această abordare se remarcă cu adevărat, este în tratamentul cancerelor rare.
În cazul cancerelor care afectează doar un mic procent din populație (de exemplu, fibrosarcomul infantil), nu „plătește” neapărat ca o companie să studieze și să dezvolte un medicament. Acest lucru nu înseamnă că nu este important, dar corporațiile tind să investească bani în moduri în care vor vedea o rentabilitate.
Cu tratamentele agnostice tumorale, totuși, companiile medicamentoase pot primi rambursare atunci când există un număr de persoane cu tipuri de cancer mai frecvente care beneficiază de un medicament. Un exemplu este Vitrakvi.
Un alt beneficiu puternic este că cercetarea promovează știința în jurul cancerului. Dar studiind căile moleculare de creștere în speranța de a găsi un tratament, sunt descoperite noi căi cu speranță pentru mai multe tratamente.
Limitări / riscuri
În timp ce terapiile agnostice tumorale pot suna ca obiectivul tratamentului viitorului, există o serie de limitări ale utilizării lor.
Nu toți cancerii răspund la fel
Chiar și atunci când două tipuri diferite de cancer au aceeași mutație care determină creșterea cancerului, răspunsul la un medicament care vizează acea mutație poate fi foarte diferit.
Un exemplu este cu mutațiile BRAF V600E. Melanoamele sau celulele leucemice cu celule păroase care adăpostesc mutația tind să fie foarte receptive la medicamentele care inhibă BRAF. În schimb, cancerele de colon care prezintă aceeași mutație nu tind să răspundă la inhibitorii BRAF.
Două tipuri de cancer care au aceeași mutație conducătoare ar putea necesita tratamente foarte diferite pentru a controla creșterea.
O altă limitare este că testarea genomică nu a devenit încă de rutină pentru toate persoanele, chiar și cu tipuri de cancer în care acest lucru ar fi recomandat cu tărie (de exemplu, cu cancer pulmonar cu celule mici). Cu unele tipuri de cancer, în special cele care sunt observate rar, pot exista puține date cu privire la caracteristicile moleculare comune prezente.
Cel mai adesea, utilizarea unor medicamente mai noi, în special a tratamentelor agnostice tumorale, este disponibilă numai printr-un studiu clinic. Nu numai că participarea la studiile clinice este mult prea scăzută în Statele Unite, dar există diferențe semnificative în ceea ce privește participarea, ceea ce face ca evaluarea tratamentelor în funcție de vârstă, rasă, sex și mai dificilă.
Dezvoltarea necesită și timp. Potrivit unui studiu, timpul mediu de la descoperirea medicamentului la testare și aprobare în Statele Unite este de 15 ani. Și chiar și atunci când aceste tratamente ating niveluri avansate în studiile clinice, acestea pot ajuta doar o minoritate de oameni.
În cele din urmă, majoritatea tratamentelor noi pentru cancer sunt acum la prețuri într-o gamă care nu este durabilă.
Un cuvânt de la Verywell
Tratarea cancerelor pe baza caracteristicilor moleculare nu este nouă, dar utilizarea acestor tratamente în mai multe tipuri de cancer poate fi aproape considerată medicament de precizie pe steroizi.
În timp ce originea unui cancer (histologie) va rămâne importantă, începând să se concentreze tratamentul asupra caracteristicilor moleculare (genomică și anomalii imunologice etc.) promite să avanseze domeniul oncologiei în moduri care ne pot surprinde la fel de mult ca și progresele recente în terapia țintită și imunoterapie.
În același timp, este incitant să ne gândim că terapia agnostică tumorală poate duce la tratamente pentru cancerele rare (în special cele la copii) care altfel nu ar fi fost posibile.
















.jpg)