Thana Prasongsin / Getty Images
Chei de luat masa
- Există un singur tratament aprobat de FDA pentru boala de celule falciforme, dar necesită un donator frate.
- Folosind tehnologia CRISPR-CAS9, cercetătorii au avut succes în direcționarea unui comutator genetic care a oprit producția pentru o formă fetală de hemoglobină.
- CRISPR-CAS9 a permis pacienților cu seceră și beta-talasemie să fie proprii lor donatori pentru transplanturi de măduvă osoasă. Acest lucru are potențialul de a face tratamentele mai accesibile.
Editarea genelor a îmbunătățit multe domenii ale științei, de la crearea de alimente fără pesticide până la încercarea de a readuce mamutul lănos. Folosind o tehnologie numită CRISPR-CAS9, denumită în mod obișnuit CRISPR, oamenii de știință încearcă acum să remedieze erorile genetice care cauzează boli.
Un studiu din ianuarie publicat înThe New England Journal of Medicinea constatat că CRISPR ar putea forja noi tratamente pentru vindecarea tulburărilor de sânge, cum ar fi boala cu celule falciforme.
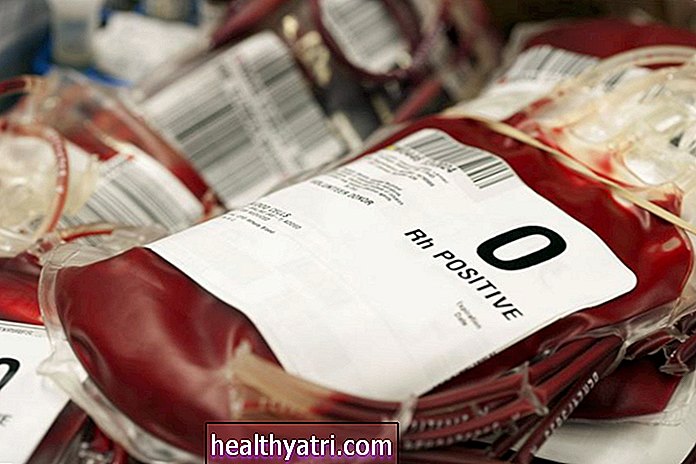
Pacienții diagnosticați cu boli de seceră au o mutație într-o genă a hemoglobinei - o proteină bogată în fier din celulele roșii din sânge. Mutația provoacă celule sanguine anormale în formă de C, cărora le este greu să transporte oxigen în alte părți ale corpului. Caracteristica sa dură și lipicioasă înfundă fluxul sanguin, ceea ce crește riscul de infecții.
Boala falciformă este o tulburare de sânge moștenită care afectează aproximativ 100.000 de americani pe an, spune Alexis A. Thompson, MD, MPH, fost președinte al Societății Americane de Hematologie și hematolog pediatru de la Școala de Medicină Feinberg de la Universitatea Northwestern, spune Verywell. În timp ce Thompson, care nu a fost implicat în studiu, spune că copiii par relativ normali la naștere, copiii încep să dezvolte probleme până la vârsta de 6 până la 12 luni.
„În grupul de vârstă mai tânăr, pacienții care prezintă durere, febră severă sau infecție necesită spitalizare, primesc medicamente foarte puternice și lipsesc de la școală", spune Thompson. „Pe măsură ce trec la maturitate, au provocări la finalizarea studiilor, la universitate sau menținerea unui loc de muncă. ” Folosind CRISPR, cercetătorii încearcă să schimbe unele dintre aceste rezultate.
Ce înseamnă asta pentru tine
Boala falciformă este transmisă unui copil atunci când ambii părinți au trăsătura falciformă. Dacă nu sunteți sigur de statutul dvs. de operator, este esențial să fiți examinat de un profesionist din domeniul sănătății. Dacă aveți boală de celule falciforme, noi tratamente folosind tehnologia CRISPR ar putea fi disponibile pentru dvs. în viitor.
Strategia genetică repornește producția de hemoglobină
Studiul a urmărit un pacient cu boală de celule falciforme și un pacient cu beta-talasemie, o afecțiune a sângelui care reduce producția de hemoglobină.
Ambii pacienți au necesitat celule stem din sânge, dar studiul a căutat să folosească celulele lor mai degrabă decât celulele de la un frate. Când celulele stem din sânge au fost luate de la pacient, cercetătorii au folosit CRISPR, care acționează ca o foarfecă moleculară, și o moleculă de ARN cu un singur ghid, CAS9, pentru a localiza o genă specifică numită BCL11A.
În acest studiu, cercetătorii au tăiat BCL11A deoarece acționează ca un comutator genetic care oprește gena care produce o formă fetală de hemoglobină. Prin reactivarea acesteia, oamenii de știință au reactivat producția de hemoglobină fetală, care a înlocuit hemoglobina lipsă sau defectă în celulele roșii din sânge ale ambilor pacienți. Orice celule bolnave rămase au fost eliminate prin chimioterapie.
Nivelurile de hemoglobină au rămas stabile luni după tratament
La șase și 12 luni după procedură, ambii pacienți au suferit aspirații de măduvă osoasă pentru a măsura numărul de celule roșii din sânge prezente în proba lor de os.
Primul pacient a fost o femeie de 19 ani diagnosticată cu beta-talasemie. La patru luni după ultimul ei transplant de măduvă osoasă cu celulele stem editate de gene, nivelurile de hemoglobină s-au stabilizat și au rămas stabile la ultima sa vizită de urmărire. Deși a suferit inițial efecte secundare grave în urma tratamentului (pneumonie și boli de ficat), acestea s-au remediat după câteva săptămâni.
Al doilea pacient a fost o femeie în vârstă de 33 de ani, cu boală de celule falciforme. La cincisprezece luni după procedură, nivelurile de hemoglobină fetală au crescut de la 9,1% la 43,2%. Nivelurile ei de hemoglobină mutantă din boala de celule secerătoare au scăzut de la 74,1% la 52,3%. În timp ce a suferit trei reacții adverse severe (sepsis, colelitiază și dureri abdominale), acestea au fost rezolvate cu tratament.
Unul dintre avantajele majore ale acestei abordări, în comparație cu formele tradiționale de tratare a acestor tulburări de sânge, este utilizarea celulelor pacientului, fără a fi nevoie de un donator.
„Celulele aceluiași pacient pot fi manipulate și pot fi transplantate fără riscul de respingere sau de a provoca reacții imune de la donator (boala grefă contra gazdă)”, Damiano Rondelli, MD, Michael Reese profesor de hematologie la Universitate din Illinois la Chicago College of Medicine, a declarat într-un comunicat.
De la publicare, cercetătorii și-au extins activitatea la încă opt pacienți - șase cu beta-talasemie și trei cu boală cu celule secera. Rezultatele lor actuale sunt în concordanță cu primii doi pacienți din studiu.
Tratamentul actual pentru boala celulelor falciforme
Tratamentul actual aprobat de FDA pentru boala de celule secera este un transplant de maduva osoasa. Cu toate acestea, această procedură necesită ca pacientul să aibă un frate al cărui țesut se potrivește perfect cu al lor.
Thompson spune că o provocare majoră a tratamentului este că unul din patru frați nu este același tip de țesut. Chiar dacă are loc transplantul de măduvă osoasă, există și efecte secundare grave ale procedurii, inclusiv eșecul grefei, boala grefă versus gazdă și moartea.
Dacă transplanturile de măduvă osoasă sunt în afara imaginii, un tratament alternativ este un transplant haploid identic. „A existat un succes cu transplanturi haploide identice în care tipul de țesut este parțial asociat, dar transplantul se efectuează într-un mod foarte diferit pentru a obține o greutate cu complicațiile dumneavoastră”, spune Thompson. Cu toate acestea, ea spune că doar o minoritate de pacienți se califică pentru acest tratament.
Datorită restricțiilor și limitărilor pentru boala de celule falciforme, Thompson spune că au existat unele discuții cu privire la faptul că pacienții servesc drept proprii donatori. În acest studiu actual, autorii privesc editarea genelor ca o cale potențială pentru acest tip de tratament.
Cum pot ajuta tratamentele genetice
Oricine poate moșteni boala falciformă, dar este deosebit de frecventă în:
- Oameni de origine africană, inclusiv afro-americani
- Hispano-americani din America Centrală și de Sud
- Oameni de origine orientală, asiatică, indiană și mediteraneană
În SUA, toți copiii născuți în țară sunt supuși screening-ului pentru boala de celule falciforme, oferind posibilități ample de tratament timpuriu. Dar mai multe scenarii fac dificilă diagnosticarea fiecărui caz. Thompson spune că familiile care au imigrat în SUA ar putea avea copii mai mari care nu au fost supuși screeningului împreună cu părinții care nu știu de statutul lor de transportator până când nu au un copil care are această afecțiune.
În ciuda imperfecțiunilor cu screening-uri, țările industrializate și-au îmbunătățit prognosticul pentru boala de celule falciforme. „Astăzi, un copil născut astăzi în Statele Unite are șanse de 95% să supraviețuiască până la vârsta adultă și același lucru este valabil și pentru alte țări cu resurse precum Regatul Unit”, spune Thompson.
Totuși, dintr-o perspectivă globală, Thompson spune că țările cu venituri mici și medii ar putea să nu ofere aceleași tratamente care sunt disponibile în prezent pentru persoanele din țări precum S.U.A.Ea spune că peste jumătate dintre copiii cu boală de celule falciforme din Africa Subsahariană nu vor trăi după vârsta de cinci ani.
Pe baza rezultatelor studiului, editarea genelor ar putea ajuta tratamentele pentru boala de celule falciforme să devină mai accesibile.
„Speranța este că acest tratament va fi accesibil și accesibil în multe țări cu venituri medii mici, Orientul Mijlociu, Africa și India și va avea un impact important în viața multor oameni din aceste zone”, a spus Rondelli. (...)








-test.jpg)